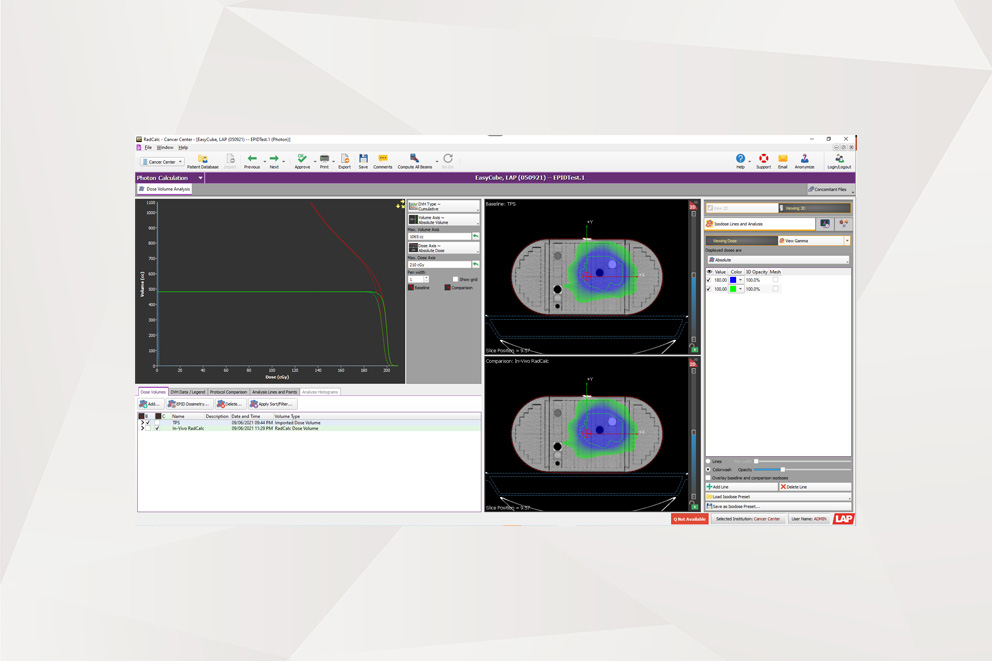
RadCalc acquiert la vérification dosimétrique in vivo
La dernière version du logiciel d’assurance qualité RadCalc de LAP mise sur la personnalisation, l’automatisation intelligente et des fonctionnalités EPID 3D pour une AQ spécifique au patient.
L’innovation axée sur la clientèle et l’amélioration continue sont à nouveau au cœur de la dernière version du logiciel de vérification secondaire RadCalc, une suite d’outils d’assurance qualité (AQ) largement utilisés qui permettent aux physiciens médicaux et aux dosimétristes de vérifier de manière entièrement automatisée et indépendante la dosimétrie de leurs systèmes de planification des traitements (SPT) de radiothérapie. La plus grande réussite de RadCalc v7.2 est l’ajout d’un module EPID 3D pour étayer l’AQ spécifique au patient et la vérification dosimétrique in vivo. Dans le même temps, la vitesse et l’efficacité du flux de travail demeurent des priorités permanentes pour l’équipe de développement de RadCalc suite à l’intégration de fonctionnalités de personnalisation pour une automatisation intelligente dans RadCalc AIR, le centre de contrôle du logiciel pour l’importation de données automatisées et les rapports.
Avec la sortie de la version 7.2, le portefeuille de calculs de RadCalc comprend désormais des vérifications de dose secondaires, avec une analyse de dose ponctuelle à l’aide d’algorithmes 3D Monte Carlo et Collapsed-Cone pour identifier les déviations cliniquement pertinentes dans le volume entier de patients ; le module EPID pour la dosimétrie avant traitement, où le logiciel reconstruit la dose à partir du plan prétraitement établi sur le scanner initial de planification du patient (ce qui permet une comparaison directe avec la dose prévue par le SPT et avec la deuxième vérification de dose 3D de RadCalc) ; et le module EPID pour la dosimétrie in vivo afin de reconstruire la dose administrée pendant le traitement, ce qui permet une comparaison directe avec la dose réelle administrée reconstruite sur le scan de planification initial afin d’évaluer les changements intrafractionnels chez le patient.
« À notre connaissance, aucun autre produit sur le marché ne peut concurrencer les fonctionnalités 3D in vivo étayées par la dosimétrie EPID de RadCalc », affirme Craig Laughton, directeur technique et fondateur du portefeuille logiciel RadCalc faisant partie de la gamme croissante de produits d’assurance qualité pour la radiothérapie de LAP. « En environnement clinique, RadCalc 7.2 permet à l’équipe de physiciens de comparer le volume entier de doses et le plan de traitement initial, pour mesurer ce qui est réellement administré in vivo durant la radiothérapie du patient. », ajoute-t-il.
Des systèmes dynamiques
De telles informations sont particulièrement importantes étant donné que les patients sont des systèmes dynamiques dans un flux constant, plutôt que dans un état permanent. Par exemple, entre les sessions de traitement, les patients peuvent prendre ou perdre du poids ; le contenu de leur estomac, de leur vessie ou de leurs intestins peut changer ; leurs organes peuvent se déplacer, pivoter ou se déformer ; et leurs tumeurs peuvent rétrécir, se déplacer ou pivoter.
Ces changements s’avèrent problématiques pour les traitements par radiothérapie traditionnels fondés sur un seul scanner au début du traitement, d’autant que la plupart des cliniques ont des capacités limitées pour pister les déformations géométriques dans l’anatomie des patients au fil du temps. En d’autres termes : un plan de traitement accordé à la simulation initiale peut rapidement devenir sous-optimal à mesure que la radiothérapie progresse de fraction en fraction sur un mois ou plus.
« Notre module EPID va capter les changements dans l’administration de la dose au fil des fractions, et permettre une conversation entre le physicien clinique et le radio-oncologue pour comprendre ce qui se passe à l’intérieur du patient », explique Laughton. « Ce dialogue peut éventuellement amener à effectuer une nouvelle imagerie et un nouveau plan pour le patient, ce qui constitue une autre étape importante vers une approche personnalisée de la radiothérapie. »
« RadCalc 7.2 mesure ce qui est réellement administré in-vivo au patient pendant la radiothérapie. »
En outre, le module EPID 3D de RadCalc a aussi un rôle important à jouer dans la prise en charge des derniers schémas de radiothérapie hypofractionnée et ultrahypofractionnée, dans lesquels une dose accrue par fraction permet de réduire considérablement le nombre total de traitements dans un délai plus court. Le but, comme toujours, est d’augmenter la précision du ciblage et de la distribution des doses, en réduisant les damages collatéraux sur les organes adjacents exposés et les structures critiques, le long d’un traitement allant d’une seule à plusieurs fractions à dose élevée.
« Avec un schéma de traitement hypofractionné, il faut savoir immédiatement si quelque chose ne va pas. Par exemple, en cas d’une erreur de la machine ou d’une configuration incorrecte pour le patient. On ne peut pas se permettre d’attendre une semaine, car une fois la semaine écoulée, le traitement aura été fait et il sera trop tard. », observe Laughton.
Automatiser pour accumuler
De façon plus générale, l’automatisation intelligente reste un élément présent à long terme sur la feuille de route du développement de RadCalc, et donne aux physiciens médicaux la capacité d’optimiser les processus selon leurs propres besoins cliniques, en personnalisant par exemple les balises DICOM pour déclencher des actions, et de nouvelles mises en page pour de meilleurs flux de travail. « Bien que l’on considère l’automatisation définie par l’utilisateur comme un facteur de différenciation clé », explique Carlos Bohorquez, responsable produit chez RadCalc, « en fin de compte, l’automatisation est là pour assurer la sécurité des patients et réduire les erreurs humaines et le fardeau des ressources cliniques associées aux tâches manuelles d’assurance qualité. »
Selon Bohorquez, la version 7.2 incorpore des personnalisations importantes dans l’outil d’importation et d’analyse RadCalc AIR pour rationaliser les flux de travail dans l’environnement clinique (p. ex. l’importation/exportation de protocoles cliniques, ou de critères de tolérance spécifiques pour chaque plan de traitement fondés sur les balises DICOM que le SPT de l’utilisateur peut exporter). « C’est un processus en constante évolution qui apporte aux cliniciens une véritable automatisation pour les technologies de radiothérapie existantes et émergentes », explique-t-il.
« En fin de compte, l’automatisation est là pour assurer la sécurité des patients et réduire les erreurs humaines. » human errors.”
C’est effectivement le cas du nouveau module EPID 3D de RadCalc, qui importe les fichiers de données ou d’images EPID nécessaires pour les traiter avant de les envoyer au moteur de dosage Collapsed-Cone pour calculer la dose. « La solution qui s’appuie sur le module EPID doit être davantage automatisée pour que l’équipe de physiciens puisse l’utiliser de manière adaptative et hors ligne, en éliminant les interventions manuelles dans l’interface utilisateur de RadCalc », explique Bohorquez. « Ce travail sera au cœur de notre prochaine version à paraître dans quelques mois, qui augmentera l’impact clinique et opérationnel de cette fonctionnalité. »
Une autre priorité pour l’équipe de développement de RadCalc est d’exploiter les fonctions de script des principales offres de SPT. « En réalité, il s’agit de changements que nous mettrons en œuvre en dehors de RadCalc pour rendre les outils d’automatisation du logiciel encore plus puissants pour l’utilisateur final en clinique. », conclut Bohorquez.
Retrouvez l’article d’origine sur le site de Physics World.